8 апреля 2013 года компания «Гилеад» подала заявку на регистрацию препарата Софосбувир, предназначенного для лечения вирусного гепатита С, в Управление по контролю за пищевыми продуктами и лекарственными средствами США (FDA). Согласно данным в заявке, софосбувир используется в полностью пероральной терапии ВГС у пациентов с генотипами 2 и 3, а также в комбинации с пегилированными интерферонами и рибавирином у ранее не леченных пациентов с генотипами 1, 4, 5 и 6.
Компания планирует подать заявку на регистрацию софосбувира в других регионах, в том числе в ЕС, во втором квартале 2013 года. Европейское агентство лекарственных средств (EMA) приняло заявку на ускоренное рассмотрение регистрационного досье софосбувира. Обычно эта процедура применяется для лекарственных средств, которые потенциально имеют существенное преимущество над уже доступными на рынке продуктами, а также представляют особую важность для общественного здравоохранения.
Софосбувир относится к антивирусным препаратам прямого действия, класс нуклеотидных ингибиторов NS5B. Это не первый антивирусный препарат прямого действия для лечения ВГС, поданный на регистрацию. Напомним, не так давно компания Janssen подала заявку на регистрацию препарата симепревир — ингибитор протеазы NS3/4A для лечения ВГС,
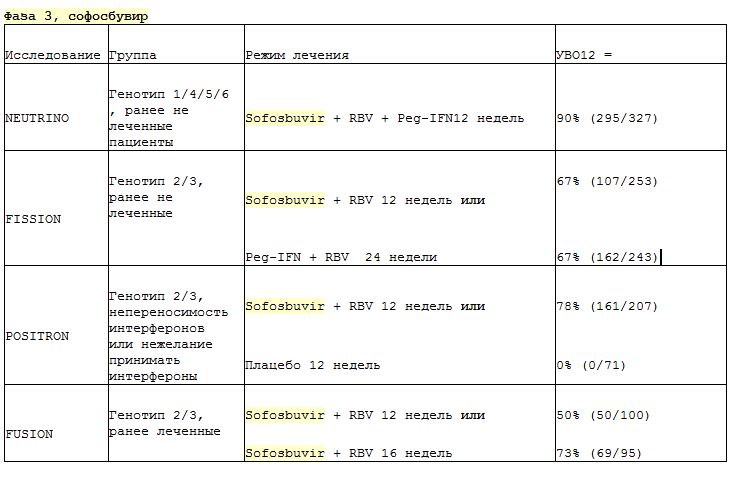
Данные испытаний фазы 3 приведены в таблице ниже, подробные данные доступны на английском.


Оставить комментарий